ヒュッケル分子軌道法ってなに?|考え方と解き方をやさしく解説
共役分子や芳香族分子は、なぜ特別に安定なのでしょうか?
「電子が非局在化しているから」と習いますが、どのように考えたらよいでしょうか?
その“見えない電子の広がり”を、シンプルな計算で説明できるのがヒュッケル法(Hückel法)です。
ヒュッケル法は、量子化学の中でも特に直感的に理解しやすい分子軌道モデルで、
- 共役による安定化
- 芳香族性の理由
- π電子の振る舞い
を簡単に説明できます。
この記事では、ヒュッケル法の考え方をざっくり解説していきます。
ヒュッケル分子軌道法とは?
ヒュッケル分子軌道法 (ざっくり)
π電子系を対象とする簡易的な分子軌道法
ヒュッケル法は、分子中のπ電子のエネルギーや分布を簡易的に求める分子軌道法です。
分子軌道(Molecular Orbital, MO)を計算するには、シュレディンガー方程式を解く必要がありますが、多原子系では解析的に解くことができません。
そこで、「π電子のことだけ考えれば、だいたいの性質はわかるよね!」と割り切ったのがこのヒュッケル法です。

分子軌道法の基本的な考え方に関しては、以下の記事で解説しています。合わせて確認してください。
ヒュッケル法の基本的な考え方
ヒュッケル法では、計算の簡略化のため近似を行います。
π電子だけを切り離して考える(σ-π分離)
ヒュッケル法ではσ電子は考えません。
- σ結合:分子骨格を作る
- π結合:エネルギーや反応性を左右する
と割り切ります。
共役や芳香族性の本質はπ電子の振る舞いにあるため、この近似でも本質を外しにくいのがポイントです。
LCAO近似(原子軌道の線形結合)
ヒュッケル法はLCAO(Linear Combination of Atomic Orbitals)の考え方に基づきます。
「分子軌道(電子の通り道)は、それぞれの原子が持っている軌道を足し算して作ろう」という考え方です。
ヒュッケル法では分子軌道Ψは、原子軌道φの線形結合で表されると仮定します。
φ:各炭素のp軌道
c:重み係数
積分の簡略化
本来の分子軌道法では、多くの積分計算が必要になります。
ヒュッケル法ではこれを単純化します。
重要なのは次の3種類だけです。
(1) クーロン積分 (α)
クーロン積分 α は、電子がある原子の p 軌道に局在しているときのエネルギーを表します。
いわば「その原子上に電子がいるときの基準エネルギー」です。
ヒュッケル法では、すべての炭素原子で同じ値をとると仮定します。
クーロン積分αは負の値を取ります。
(2) 共鳴積分 (β)
共鳴積分 β は、π電子が2つの原子上に分布する際のエネルギーを表します。
結合し合う原子間でのみゼロでない値を持ち、 β で表します。
共鳴積分βは負の値を取ります。
(3) 重なり積分(S)
重なり積分は、原子軌道同士がどれくらい重なっているかを表す量です。
実際の分子では、隣接する原子の軌道は有限の大きさで重なっています。
しかしヒュッケル法では、計算を簡単にするため原子軌道同士は直交すると仮定します。
すなわち、同一原子軌道の規格化積分のみを
とし、異なる原子軌道間の重なり積分
はすべて 0 とみなします。
この近似により、ヒュッケル法では重なり積分を明示的に扱わずに計算を行うことができます。
ヒュッケル法の解き方
Step 1:ヒュッケル行列を立てる
分子のつながり方に合わせて、「ヒュッケル行列」と呼ばれる図式を作ります。
- 対角成分:α
- 隣接原子間:β
- それ以外:0
というルールで行列を作ります。
Step 2:永年方程式を解いてエネルギー E を出す
数学的な処理(行列式の展開)を行い、エネルギーの解を求めます。
を解いてエネルギーEを求めます。
ここで軌道の数だけエネルギー準位が得られます。
Step3:軌道係数を求める
得られた各Eを
に代入して軌道係数cを求めます。
これにより
が決まります。
これが分子軌道の「形」になります。
軌道係数の規格化
分子軌道Ψは確率振幅を表すため、
を満たす必要があります。
ヒュッケル法では軌道の直交性とS=0(異なる原子間)近似により、
と書けます。
つまり、
係数の二乗が電子存在確率になるように調整
します。
Step 4:各軌道に電子を詰める
得られた軌道に、パウリの原理に従って電子を入れます。
これで安定性や結合次数を議論できます。
【例題】エチレンでヒュッケル法をやってみる
Step 1. ヒュッケル行列を立てる
ヒュッケル行列を設定します。
対角にクーロン積分αをおき、結合を作る原子の位置に共鳴積分βをおきます。
ヒュッケル行列は下記のようになります。
Step 2. 永年方程式を解く
ヒュッケル行列より永年方程式を立てます。
この永年方程式より、 E = α ± β
Step 3. 軌道係数の決定
エネルギーを
に代入します。
(1) E=α+βのとき 結合性軌道
規格化すると:
- 同位相の重なり
- 結合性軌道
(2) E = α-βとき 反結合性軌道
規格化すると:
- 逆位相
- 節が生じる
Step 4. 各軌道に電子を詰める
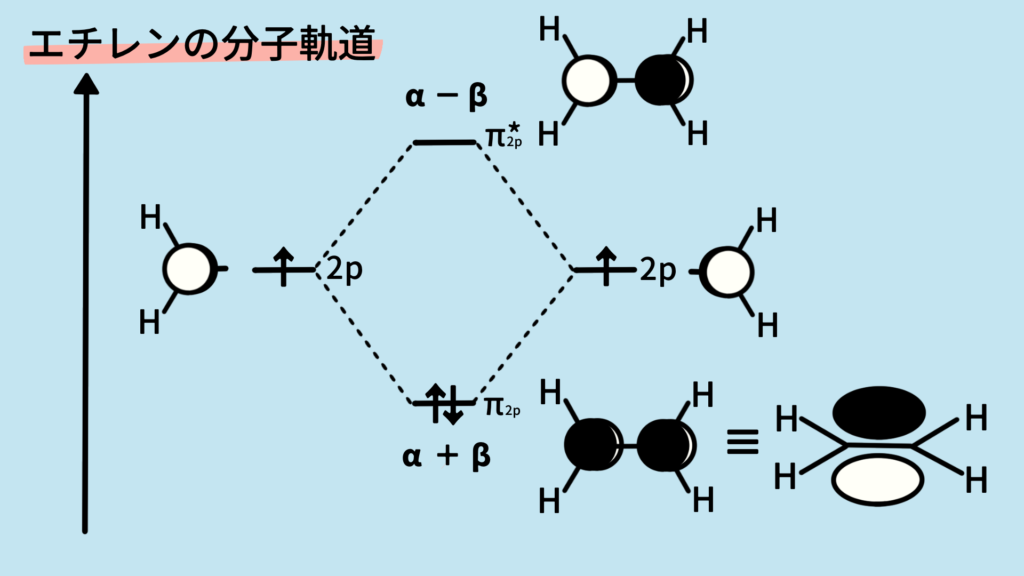
エチレンのπ電子は2個あります。
低エネルギー軌道(α+β)に2個入る
高エネルギー軌道(α−β)は空
共鳴積分βは負なので、
- 結合性軌道は α+β で安定化
- 反結合性軌道は α−β で不安定化
となります。 - 未結合の2つの炭素原子:2α
- エチレン:2α+2β
これにより、エチレンになることで、2βの安定化が得られます。
これが「π結合による安定化」の正体です。
ベンゼンのヒュッケル分子軌道
ベンゼンのヒュッケル分子軌道の算出は煩雑なため省略し、エネルギー図の確認をしましょう。
分子軌道から分かるベンゼンの安定性
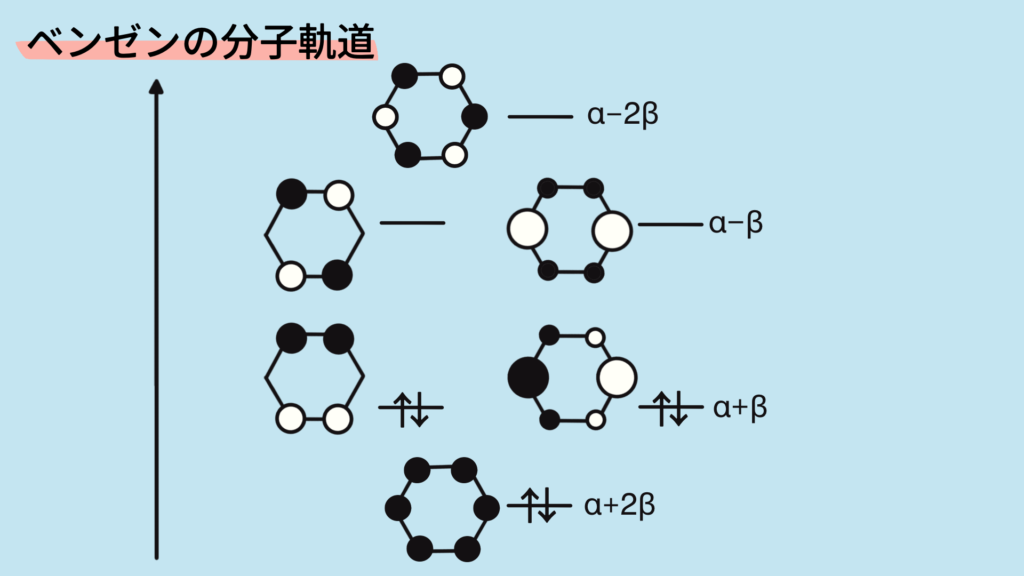
ベンゼンでは6個のp軌道が環状に結合。
エネルギー準位:
- α+2β
- α+β(2重縮退)
- α−β(2重縮退)
- α−2β
π電子6個は結合性軌道をちょうど満たします。
- 反結合性軌道が空
- 大きな安定化
これが芳香族安定性の本質です。
ヒュッケル則(4n+2則)との関係
混同されやすいですが、ヒュッケル法とヒュッケル則は別物です。
- ヒュッケル法:計算手法
- ヒュッケル則:経験則
ただし、ヒュッケル法で環状共役系を解くと、4n+2個のπ電子で安定化する理由がわかります。
まとめ
ヒュッケル法は、π電子のエネルギーと広がりをざっくり理解するための理論ツールです。
- 共役の安定化
- 芳香族性
- 電子の非局在化
を直感的に理解する入口として非常に優れています。
量子化学の第一歩として、今でも学ぶ価値のあるモデルといえるでしょう。


